
原发免疫性血小板减少症(ITP)是一种自身免疫性疾病,其诱因尚不明确,临床上表现为孤立性外周血血小板计数减少(血小板计数<100×109/L)。大多数ITP治疗策略旨在控制出血,防止血小板过早破坏(免疫抑制,脾切除术)和增加血小板生成(血小板生成素受体激动剂[TPO-RA])。
10余年来,TPO-RA被用来提高ITP患者的血小板计数,许多国家批准其作为ITP患者的二线治疗方案。尽管血小板反应良好,但大部分患者需要持续接受TPO-RA治疗以维持疗效。但一些临床研究表明TPO-RA治疗中断或停止,患者仍能获得持续缓解。一项汇总分析显示,≤1年ITP患者(n=277)和>1年ITP患者(n=634)的无治疗缓解(TFR)率分别为16%和6%,远高于初始回顾性分析结果。此外,有研究者认为罗普司亭具有额外免疫调节活性,并推测其可能影响ITP患者的免疫调节。基于此,来自瑞士的研究者开展了一项前瞻性iROM研究,在细胞、细胞因子和基因评估的基础上,分析了罗普司亭对ITP患者免疫系统的影响。
研究方法
iROM研究是一项多中心、开放标签、单臂、概念验证性研究。纳入患者为年轻成人(18-45岁)ITP患者,这些患者血小板计数<30×109/L或为一线治疗后失败、复发或出现明显副作用的高危人群。既往接受过二线治疗、存在继发性ITP风险和血栓栓塞性疾病史以及同时应用已知影响免疫系统药物的患者被排除在外。因招募困难,研究开始1年后,研究者将患者的最大入组年龄提高至60岁。
每周给予患者罗普司亭皮下注射,持续22周(起始剂量:1μg/kg)。依据产品信息基于血小板反应每周可进行剂量调整(血小板计数目标:50×109/L-200×109/L)。22-52周,停药后完全持续缓解(血小板计数>100×109/L;SROT)的患者为SROT组;22周后,需要进行增强血小板治疗的患者为复发组。没有患者血小板计数稳定在30×109/L-100×109/L且不需要接受后续治疗。无论何时减量或停药,剂量调整原则均适用。
第1、6、12、22和52周进行免疫学评估,分析辅助性T细胞(Th细胞)Th1、Th17、Th2和调节性T细胞(Treg细胞)活性间的平衡状态。根据荧光激活细胞分选术(FACS)、细胞因子水平以及mRNA表达评估免疫模式。(图1)
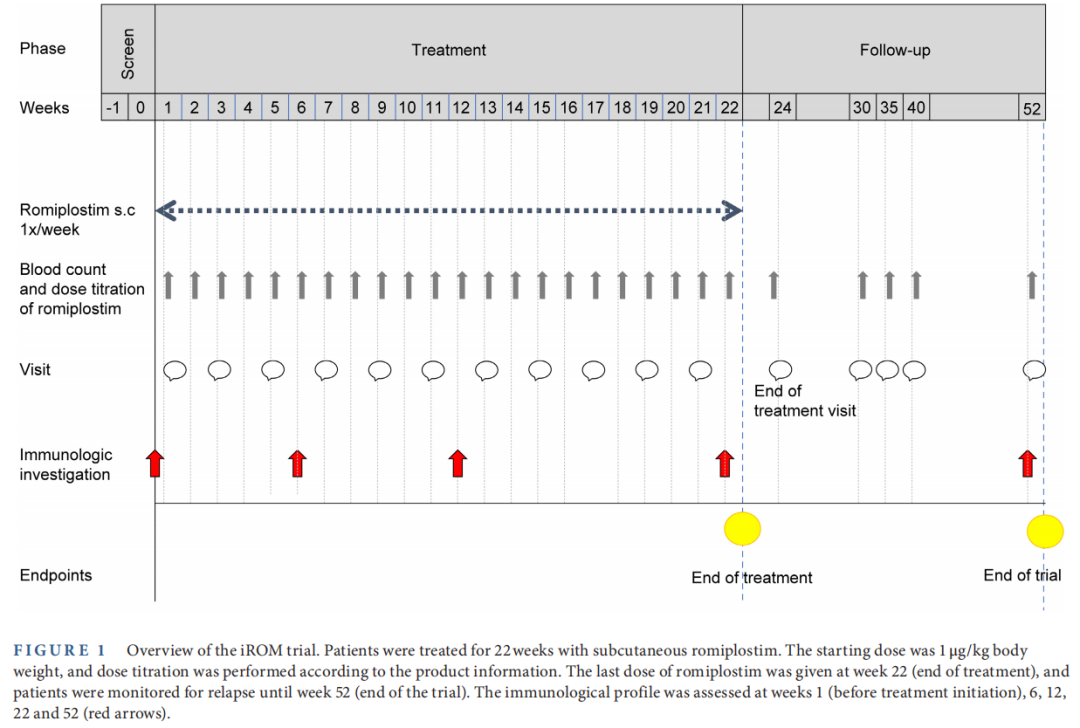
图1
研究结果
➤临床终点
2016年12月至2020年2月,该研究共纳入15例患者。2例患者因对罗普司亭反应不足或无反应被排除在外。其余13例患者中位年龄为31岁(范围:19-51岁),仅2例患者年龄>45岁。入组前患者特征详见表1。
表1

相较于复发患者,SROT患者罗普司亭滴定剂量更低,血小板计数反应更快、更强。治疗结束时,6例(67%)新诊断ITP患者在没有进一步药物治疗的情况下,维持完全和持续缓解状态直至第52周,7例患者出现复发(3例新诊断ITP,4例慢性ITP)。总之,研究结束时6/13例(46%)患者处于SROT。
➤免疫学终点
第6-52周,整体队列Treg/CD3比率均有所增加。第6-22周及第6-52周,SROT组患者Treg/CD3比率变化值更大(图2)。

图2
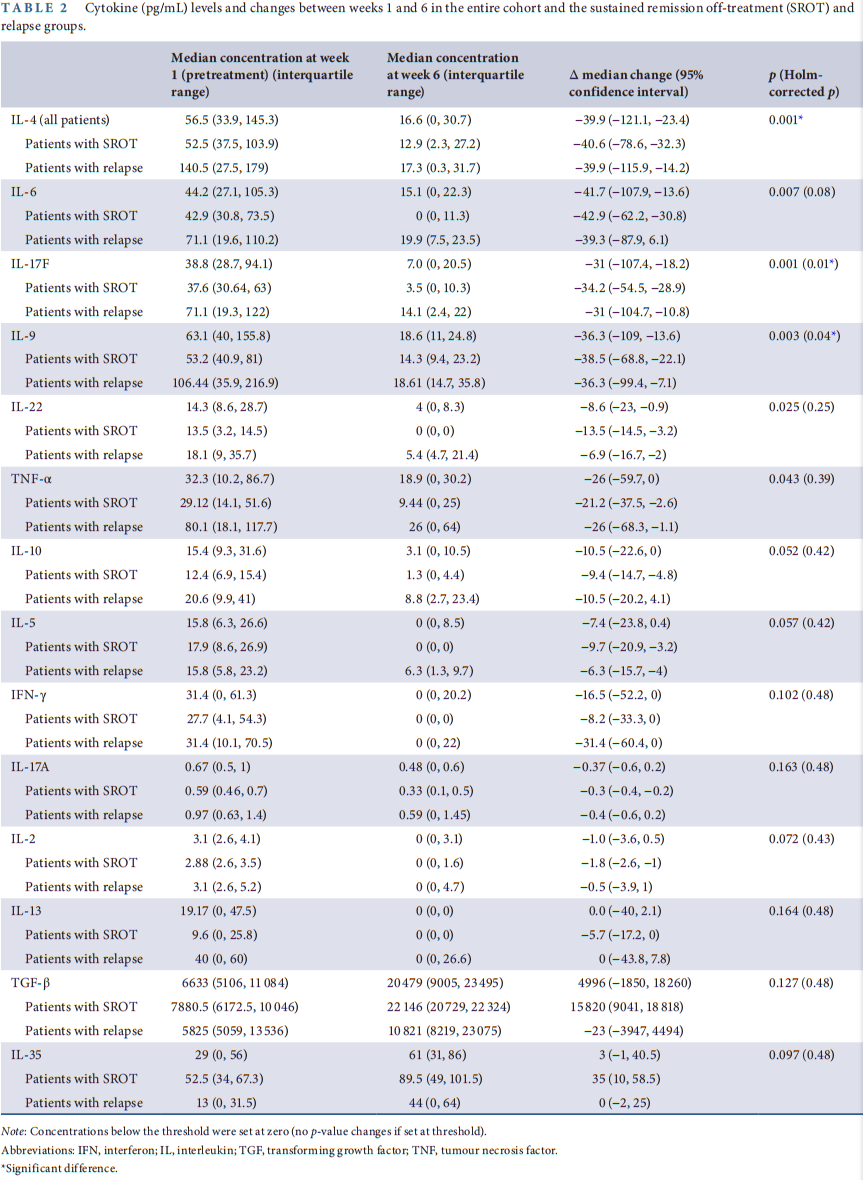
所有患者白细胞介素(IL)-4、IL-9和IL-17F水平均显著降低。第1-6周细胞因子变化情况详见表2。
表2
SROT组患者FOXP3(Treg细胞)、GATA3(Th2细胞)mRNA表达增加(图3),转化生长因子-β(TGF-β)水平升高。
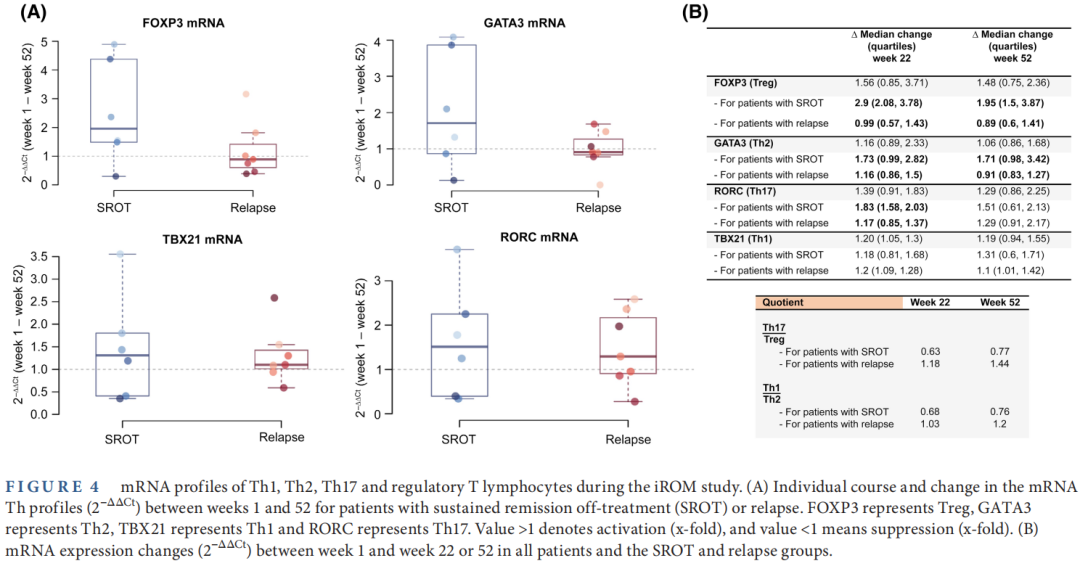
图3
小结
既往研究显示,罗普司亭能使ITP患者停药后获得持续缓解,除此之外,其免疫调节活性也备受关注。本次研究,研究者根据既往研究结果及假说,提出了罗普司亭在ITP患者免疫系统中发挥作用的机制,详见图4。结果表明,罗普司亭可以调节免疫系统,并且可能影响ITP患者预后。快速增加血小板数量可能对免疫耐受诱导十分重要。自身免疫的早期阶段可能会获得更好的结果,但需要临床研究进一步证实。
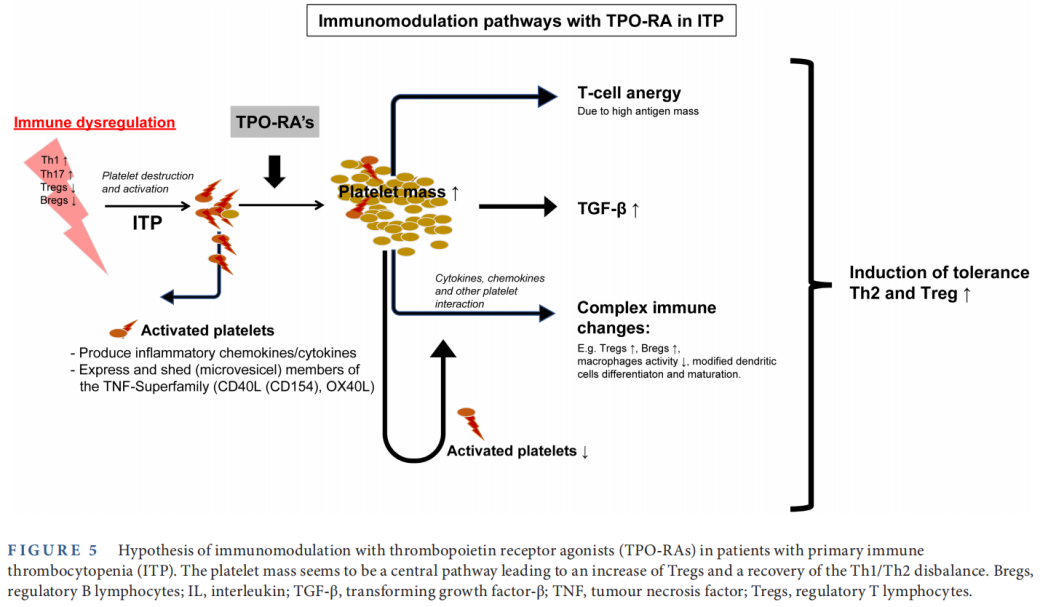
图4