
暴露于细胞毒性药物的个体具有发生治疗相关性急性髓系白血病(t-AML)、治疗相关性骨髓增生异常综合征(t-MDS)和治疗相关性骨髓增生异常综合征/骨髓增殖性肿瘤(t-MDS/MPN)的风险。 这些情况是疾病病程中的不同阶段,在2008年世界卫生组织(WHO)分类系统中将其归类为治疗相关性髓系肿瘤(t-MN)。这类疾病患者具有异质性、定义不明性,且与原发性AML、MDS或MDS/MPN患者相比,中位生存期更短。
有关t-AML、t-MDS、t-MDS/MPN的流行病学、诊断和治疗不再赘述,鉴于治疗相关性髓系肿瘤(t-MN)往往预后不良,为便于临床医师评估预后,本文单独对治疗相关性髓系肿瘤(t-MN)基本特征、预后评价进行综述。
一、治疗相关性髓系肿瘤(t-MN)基本特征
1. 疾病构成
治疗相关性髓系肿瘤(t-MN)常因实体瘤、造血系统疾患放疗、化疗或使用其他细胞毒作用有关,图1从常见的实体瘤及造血系统疾患阐述了t-MN的常见病因。
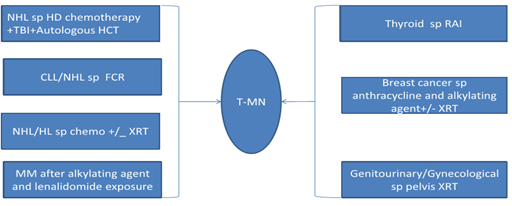
图1 继发治疗相关性髓系肿瘤(t-MN)的常见实体瘤及造血系统疾患
治疗相关性骨髓增生异常综合征(t-MDS)总体较原发MDS(de novo MDS,d-MDS)预后差,但鉴于部分t-MDS仍为惰性病程,故对t-MDS进行预后分层,仍有临床指导意义。以往MDS预后评估模型中,常未涉及相关性骨髓增生异常综合征(t-MDS。在2017年美国一项多中心研究中,分别比较了国际预后积分系统(IPSS)、修订IPSS (IPSS-R)、MD Anderson 全球预后评估系统(MPSS)、WHO预后积分系统 (WPSS)及t-MDS预后评价系统(TPSS)在t-MDS预后估测价值。共有1950名MDS患者纳入研究,其中370例(19%) 为t-MDS。结果显示:t-MDS中位生存期明显短于d-MDS (19 vs 46 个月, P<0.005)。应用Akaike信息标准(AIC) 比较上诉各项预后评价系统,发现AIC 积分 (数值低代表价值高) 为2316 (MPSS)、2343(TPSS)、2343(IPSS-R)、2361(WPSS) 及2364(IPSS)。MPSS、TPSS及 IPSS-R在治疗相关性骨髓增生异常综合征(t-MDS)可以有效评估预后,指导分层治疗。
二、治疗相关性髓系肿瘤(t-MN)预后评价策略
1. 整体状态评估
治疗前评估参照原发性AML。此外,应在早期阶段寻找异基因造血干细胞移植(allo-HSCT)的HLA匹配供体。具备以下基线情况者预后不佳:
➤ 既往治疗相关的脏器功能不全
➤ 残存正常造血干细胞数量/质量低
➤ 骨髓基质已受损害
➤ 长期免疫抑制状态
➤ 耐抗生素微生物的定植
➤ 不良细胞遗传学异常的发生率增加
➤ 多重耐药表型的频繁表达
➤ 原发性恶性疾病的持续存在
2. 一般状况和日常生活活动能力的评估
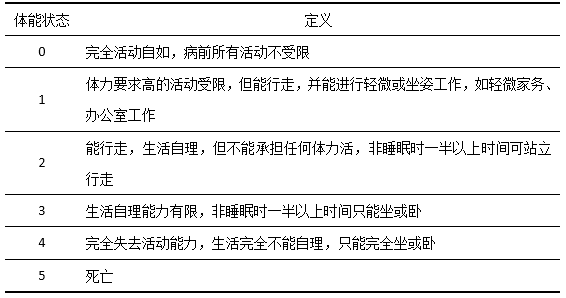
美国东部肿瘤协作组(ECOG)评分系统评定的一般状况和日常生活活动能力,为关于t-MN患者能否足够健康从而使其能在典型强化化疗诱导方案(用于AML患者)中存活提供指导意见(表1)。完全能自由走动的患者(即,ECOG为0分或1分)很可能耐受诱导化疗,而日间至少一半时间卧床的患者(即,ECOG为3分或4分)在诱导化疗过程中死亡的风险较高。
表1:美国东部肿瘤协作组ECOG行为状态分级
3. 核型危险分层
常用的一种危险分层系统如下:
➤ 良好:t(8;21)、inv(16)、t(15;17)
➤ 中等:正常、t(9;11)、其他的异常核型(不属于预后良好和预后不良)
➤ 不良:3q21q26异常、del(5q)、del(7q)、t(6;9)、其他11q23异常、12p异常、17p异常、5号或7号染色体单体、8号或13号三体或复杂异常核型[即至少存在3种不相关的异常,不包括同时有t(8;21)、inv(16)和t(15;17)的病例。
Ganser A等近期发现:15%的t-AML病人融合基因突变良好,但50%存在不良细胞遗传学改变;其中33% t-AML及t-MDS患者存在TP53基因突变,且TP53基因突变者异基因造血干细胞移植(allo-HSCT)缓解率低;微小残留病(MRD)监测有助于治疗相关性髓系肿瘤(t-MN)的异基因造血干细胞移植(allo-HSCT)实践。
4. 常用MDS预后评分系统
(1)IPSS预后评分(表2)
表2 IPSS预后评分
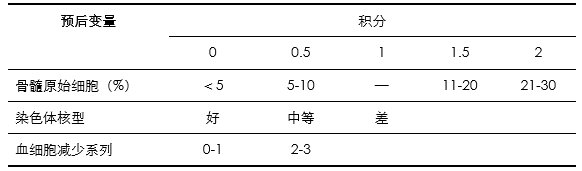
预后好核型:正常,-Y,del(5q),del(20q);预后中等核型:其余核型;预后差核型:复杂核型(≥3个)或7号染色体异常。
血细胞减少系列:中性粒细胞数目<1.8×109 /L;HGB<100g/L;PLT<100×109 /L。
分级:低危组0分,中危-1组0.5-1分,中危-2组1.5-2分,高危组>2分。
(2)IPSS-R预后评分(表3)
表3 IPSS-R预后评分

细胞遗传学极好:—Y,11q-;好:正常核型,5q-,12p-,20q-,5q-附加另一种异常;中等:7q-,+8,+19,i(17q),其他一个或两个独立单克隆的染色体异常;差:-7,inv(3)/t(3q)/del(3q),-7或7q-附带另一种异常,复杂异常(3个);极差:复杂异常(>3个)。分级:极低危:≤1.5分;低危:>1.5-3分;中危:>3-4.5分;高危:>4.5-6分;极高危:>6分。
(3)WPSS预后评分(表4)
表4 WPSS预后评分
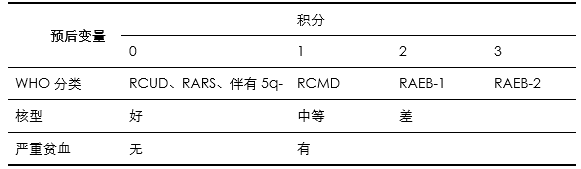
核型:预后好核型:正常,-Y,5q-,20q-;预后中等核型:其余核型;预后差核型:复杂核型(≥3个)或7号染色体异常。严重贫血:男性<90g/L,女性<80g/L。
预后分级:极低危:0分;低危:1分;中危:2分;高危:3-4分;极高危:5-6分。
(4)TPSS预后评分(表5)
危险因素:年龄(>65岁),ECOG一般状态评分(2-4分),细胞遗传学(7q-或复杂核型),MDS的WHO分型(RARS、RAEB-1和RAEB-2),血红蛋白水平(<11g/dL),血小板计数(<50×109/L),输血依赖。
低危:0-2个危险因素,中危:3-4个危险因素,高危:5-7个危险因素。
表5 TPSS预后评分

5. 新型t-MN预后评估模型
Quintas-Cardama et al近期阐述了一种评估t-MDS向AML转化的预后评估模型。以下因素为短生存期的独立预测因子:年龄> 65 岁(HR 1.63)、ECOG 2-4 (HR 1.92、细胞遗传学 (-7 和/或 复杂核型) (HR 2.47)、WHO MDS 分型 RARs 或 RAEB-1/2 (HR 1.92)、血红蛋白 < 11 g/dl (HR 2.24)、血小板 < 50 × 109/L (HR 2.01) 及输血依赖 (HR 1.59)。预后分层评估:良好 (0-2 个危险因素)、中等 (3-4 个危险因素) 、差 (5-7个危险因素)。其评估为良好、中等、差的中位生存期分别为34、12及5个月,其1年无AML生存率为96%、84%及72%(p = 0.001)。
6. 造血干细胞移植相关的t-MN预后因素
基因表达紊乱在t-MDS发病之前可被早期检测到。伴有del (5q) 的MDS病人可见50%的CD34+ mRNA水平降低;而APC基因不足可促成造血干细胞(HSC)的隐性丢失;t-MDS存在其遗传易感性,一项基因组序列分析发现3种单核苷酸多态性(SNPs)与伴有7号或5号染色体异常的t-MDS/AML有关,而烷化剂诱导的t-AML则与多种基因异常通路共同作用相关;在de novoMDS 及AML中,仅10%病人存在p53基因突变,但在t-MDS中其比例则高达28%-30%,且后者通常与-7、-5或其他复杂染色体核型产生相关,7号染色体异常可引起端粒缩短而造成基因内源性不稳定,产生不良预后;在小鼠试验中发现Sbds基因丢失可导致成骨细胞祖细胞发育障碍,引起脊髓发育不良,细胞微环境的紊乱可诱发造血干细胞缺陷而产生t-MDS;活性氧(ROS)的大量产生造成线粒体功能改变,加速DNA损伤,从而在细胞发育、蛋白质合成、DNA修复、检查点反应等层面产生病理生理改变,诱发t-MDS,而这些因素应当在移植前预处理时加以考虑。
三、临床实例及启示
1. 不同基线条件下t-MN病人预后差异及IPSS-R积分评估价值
2017年爱尔兰的1项单中心回顾性分析(图2)显示:(a)t-MN总生存率(OS)随时间而陡然下降,5年生存率仅20%左右;(b)实体肿瘤继发t-MN者5年生存率约为50%,而造血系统疾病继发t-MN者5年生存率不足30%(p=0.127);(c)IPSS-R积分为高危、极高危者,5年生存率仅10%,而IPSS-R积分为极低、低或中危者5年生存率超过30%(p=0.025)。提示IPSS-R积分系统在t-MN治疗过程中具备较高预后评估价值。
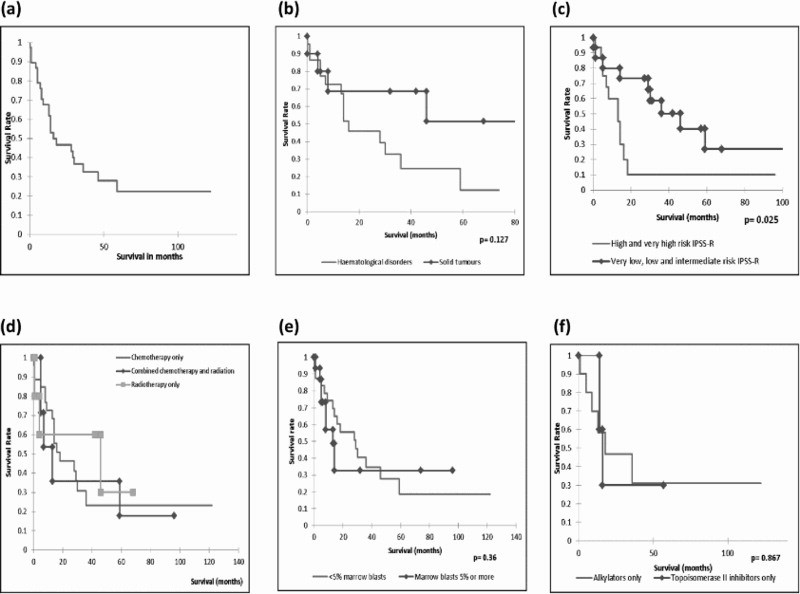
图2 39例t-MN病人生存曲线分析
2. 原发性乳腺癌患者继发t-MDS预后
2016年,Malmgren JA总结了1项纳入11684例原发性乳腺癌患者继发t-MDS的流行病学、治疗及预后研究。结果显示:确诊27例t-MDS患者,其中仅2例干细胞移植后无病生存;原发性乳腺癌t-MDS发病率是普通人群的30倍(RR 31.8, 95% CI 15.0,60.8),且自t-MDS发病至死亡中位生存时间明显缩短(中位生存时间: <55:8月,55-74: 26月,75+:23月);通常预后较差。
3. 中枢神经系统肿瘤与t-MN
原发性颅脑肿瘤继发t-MN者罕见,其发生主要与使用烷化剂、拓扑异构酶II抑制剂有关。不过,随着烷化剂的使用和患者生存期延长,烷化剂相关的迟发型毒性反应、骨髓抑制作用愈发明显,患者可能因此继发t-MN。目前中枢神经系统肿瘤生存率仍偏低,患者往往尚未继发t-MN便因原发肿瘤而丧生。然而,可预见的是,随着原发中枢神经系统诊治水平的提升,其继发t-MN者将会增多,这部分的病人有待前瞻性试验评估其继发t-MN风险。
四、结语
综上,诸多因素影响治疗相关性髓系肿瘤(t-MN)预后,如治疗前器官功能障碍、造血干细胞缺失、骨髓基质受损、慢性免疫抑制状态、反复输血依赖等。根据国际预后积分系统(IPSS)、修订IPSS (IPSS-R)、MD Anderson 全球预后评估系统(MPSS)、WHO预后积分系统 (WPSS)及t-MDS预后评价系统(TPSS)有助于t-MDS预后评估,结合病人整体状态、活动能力及核型危险分层有助于t-AML预后指导,新型t-MN预后评估模型值得探索。
值得一提的是,在治疗相关性髓系肿瘤(t-MN)中,AML-M3却有罕见的良好预后。t-AML-M3有着独特的临床表现,其染色体核型、分子生物学特点均与其他t-AML截然不同。Sang Hyuk Park认为这与t-AML-M3特有的染色体核型有关,并认为染色体核型是t-AML的最强预后评估因子。复杂染色体核型较单一核型预后差(7.9 vs. 31.3月,P=0.008) 及DFS (9.5 vs. 38.6月,P=0.046)。
目前对于t-MN尚无标准化的治疗方案,异基因造血干细胞移植(allo-HSCT)被认为是t-MN的唯一治愈手段。但由于既往放、化疗对造血干细胞的损伤、药物对脏器的累积毒性作用及供者选择使患者接受allo-HSCT治疗受到限制,因此移植前早期HLA配型是必要的。但即使接受allo-HSCT治疗,t-MN患者的预后仍极差。因此,t-MN的治疗应遵循个体化原则。
参考文献
[1] Abou Zahr A, Kavi AM, Mukherjee S. Therapy-related myelodysplastic syndromes, or are they? Blood Rev. 2016 24(12). S0268-960X.
[2] Zeidan AM, Al Ali N2, Barnard J. Comparison of clinical outcomes and prognostic utility of risk stratification tools in patients with therapy-related vs de novo myelodysplastic syndromes: a report on behalf of the MDS Clinical Research Consortium. Leukemia. 2017;24-33.
[3] Godley LA, Larson RA, Therapy-related myeloid leukemia. Semin Oncol. 2008;35(4):418.
[4] Larson RA, Wernli M, Le Beau MM,et al. Short remission durations in therapy-related leukemia despite cytogenetic complete responses to high-dose cytarabine.Blood. 1988;72(4):1333.
[5] Ganser A, Heuser M. Therapy-related myeloid neoplasms. Curr Opin Hematol. 2017;24(2):152-158.
[6] Candelaria M, Dueñas-Gonzalez A. Therapy-related myelodysplastic syndrome. Expert Opin Drug Saf. 2015;14(5):655-65.
[7] Quintás-Cardama A. A prognostic model of therapy-related myelodysplastic syndrome for predicting survival and transformation to acute myeloid leukemia. Clin Lymphoma Myeloma Leuk. 2014;14(5):401-10.
[8] Ravi Bhatiaand H, Joachim Deeg. Treatment-Related Myelodysplastic Syndrome - Molecular Characteristics and Therapy. Curr Opin Hematol. 2011 ; 18(2): 77-82.
[9] Maung SW, Burke C, Hayde J. A review of therapy-related myelodysplastic syndromes and acute myeloid leukaemia (t-MDS/AML) in Irish patients: a single centre experience. Hematology.
[10] Malmgren JA, Calip GS, Pyott SM, Therapy-related myelodysplastic syndrome following primary breast cancer. Leuk Res. 2016;47:178-84.
[11] Baehring JM, Marks PW. Treatment-related myelodysplasia in patients with primary brain tumors. Neuro Oncol. 2012;14(5):529-540.
[12] Sang Hyuk Park, Hyun-Sook Chi, Young-Uk Cho. Evaluation of prognostic factors in patients with therapy-related acute myeloid leukemia. Blood Res 2013;48:185-92.