
2025年中国临床肿瘤学会(CSCO)指南大会已在山东济南顺利召开。在会议期间,《CSCO
CSCO指南重磅更新:CD20/CD3双抗在DLBCL二线治疗中获高度认可
本次指南会公布了《CSCO淋巴瘤诊疗指南(2025)》(以下简称“2025版指南”),对比2024版,2025版指南基于循证医学证据,及时对R/R DLBCL治疗推荐进行了部分更新:对于首次复发/进展的不适合移植DLBCL患者,新增格菲妥单抗联合GemOx作为Ⅱ级推荐(2A类),新增
表1 2025版指南对于R/R DLBCL治疗推荐
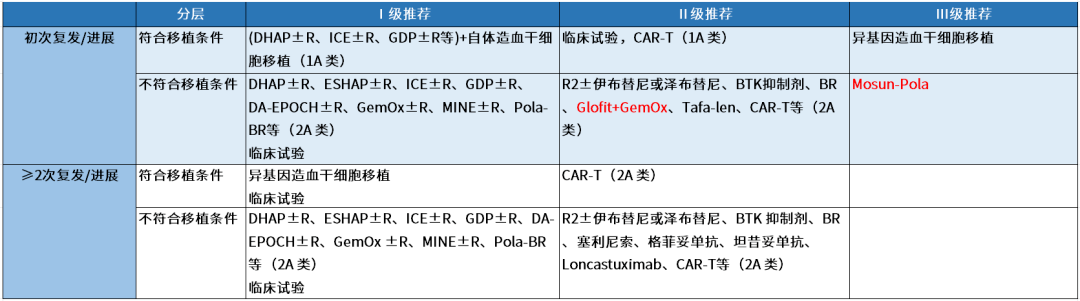
* Glofit-GemOx,格菲妥单抗、吉西他滨、奥沙利铂;Mosun-Pola,维泊妥珠单抗+莫妥珠单抗
2025版指南针对R/R DLBCL的注释部分也进行了更新,注释中将CAR-T和双特异性抗体同归类为T细胞免疫疗法进行描述,凸显了这一创新疗法的突破性价值;并新增“格菲妥单抗单药或者联合GemOx固定周期(无论单药或联合方案,至多12个周期)给药治疗显示出快速持久缓解,可进一步提升患者生存”,修改新增“莫妥珠单抗等新药单用或联合治疗亦体现初步疗效”。以上更新均体现了专家组对CD20/CD3双抗的高度认可。
指南引领、循证奠基,多项研究力证CD20/CD3双抗方案治疗获益
双抗+化疗突破瓶颈:在不适合移植R/R DLBCL患者中,对比二线免疫化疗,格菲妥单抗联合GemOx获显著OS优势[2-4]
2025版指南将格菲妥单抗+GemOx方案列为不适合移植的初次复发/进展DLBCL治疗的Ⅱ级推荐,是基于一项随机、多中心、全球Ⅲ期STARGLO研究数据,该研究结果于2024年入选EHA会议Late-Breaking Abstracts(最新突破进展摘要,简称LBA),随后全文发表于The Lancet(IF:98.4)杂志。
STARGLO研究评估了来自全球62家中心接受格菲妥单抗联合GemOx(Glofit-GemOx,n=183)与
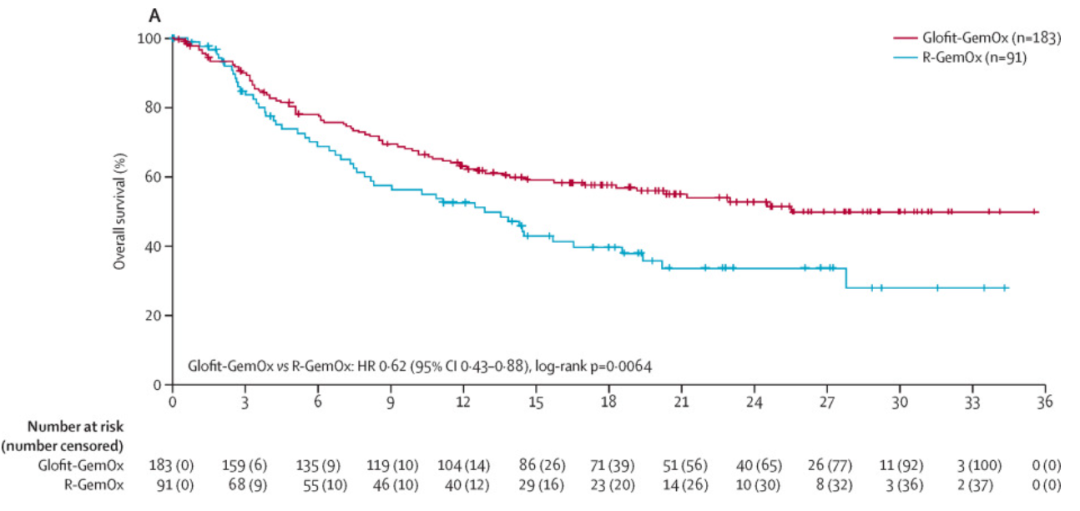
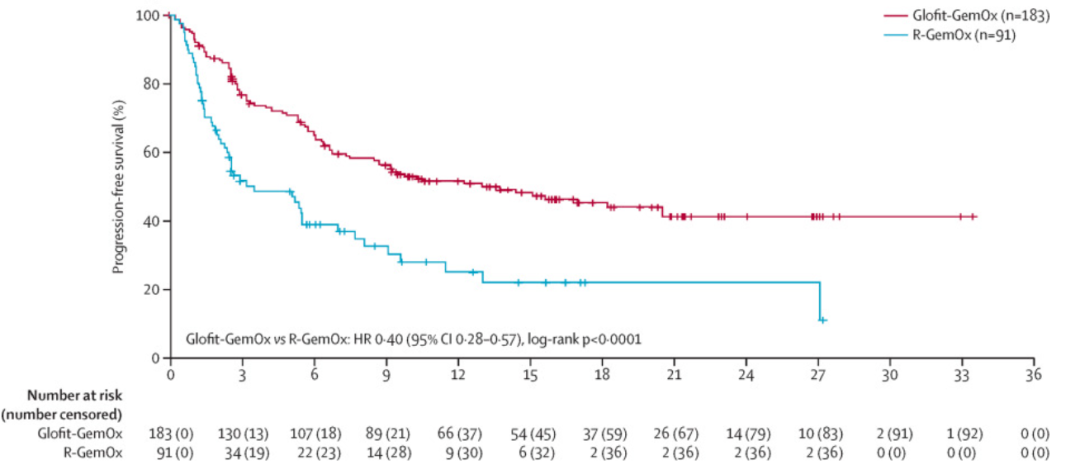
图1 STARGLO研究更新分析中,意向治疗人群的OS(A)、IRC评估的PFS(B)的Kaplan-Meier曲线
在STARGLO研究的患者报告结局(PRO)中,两组的健康相关生活质量(HRQoL)核心指标(疲劳、身体功能及淋巴瘤中位至症状恶化时间)总体相当,但格菲妥单抗组患者更早缓解疼痛和改善淋巴瘤症状,且患者报告的疼痛和淋巴瘤症状负担较轻[3]。此外,结合该治疗方案在生存获益方面的显著优势,以及二线及后线治疗场景下的成本分析显示其累计支出在T细胞免疫疗法中较低[4],提示Glofit-GemOx在R/R DLBCL治疗中具有潜在优势。
ADC+双抗协同增效:维泊妥珠单抗+莫妥珠单抗治疗R/R LBCL患者可持久缓解[5,6]
2025版指南新增维泊妥珠单抗+莫妥珠单抗(mosun–pola)作为Ⅲ级推荐,是基于一项Ⅰb/Ⅱ期GO40516研究数据。初步研究结果显示,固定疗程的莫妥珠单抗(静脉注射,IV)联合维泊妥珠单抗方案治疗R/R LBCL患者持久缓解,中位随访23.9个月后,中位DoCR未达到,中位PFS为11.4个月[5]。在2024 ASH会议报道的最新数据显示,莫妥珠单抗皮下剂型(SC)联合维泊妥珠单抗相较R-Pola方案亦可提高R/R LBCL患者的缓解率,在纳入的80例患者中,莫妥珠单抗+维泊妥珠单抗组ORR(77.5% vs 50%)和CR率(57.5% vs 35%)显著优于对照组,中位DOR分别为未达到vs 10.1个月,降低了55%疾病进展或死亡风险(P=0.025)。在安全性方面,维泊妥珠单抗联合莫妥珠单抗的停药率更低(2.5% vs 5.1%),SAE与对照组相当,且CRS发生率较低(10%,均为1-2级)[6]。
*R-Pola,利妥昔单抗+维泊妥珠单抗;R/R LBCL,复发/难治性大B细胞淋巴瘤;SAE,严重不良事件;ORR,缓解率;DOR,缓解持续时间;DoCR,完全缓解持续时间;CRS,细胞因子释放综合征