
一线治疗后的复发/难治性(R/R)大B细胞淋巴瘤(LBCL)患者如果无法接受巩固性大剂量化疗(HDCT)和造血干细胞移植(HSCT),其预后不良,且可选择的治疗方案有限,利妥昔单抗、吉西他滨和奥沙利铂(R-GemOx)是这种情况下常用的免疫化疗方案。
01 R-GemOx联合纳武利尤单抗 vs R-GemOx作为不适合移植的R/R LBCL患者二线治疗的疗效
这项开放标签的III期NIVEAU研究(NCT03366272)旨在评估R-GemOx联合纳武利尤单抗治疗R/R LBCL患者的疗效和安全性,纳入了一线免疫化疗难治或一线免疫化疗后复发的R/R LBCL成人患者,并且根据医生的评估和以下至少一项标准,不适合接受HDCT/HSCT:年龄>65岁;造血干细胞移植合并症指数(HCT-CI)评分>2分;自体造血干细胞移植(ASCT)后复发且不适合接受异基因造血干细胞移植。治疗包括8个周期的R-GemOx(A组)或8个周期的纳武利尤单抗+R-GemOx,随后纳武利尤单抗维持治疗,总共治疗长达1年,或者直至疾病进展或出现不可接受的毒性(B组)。主要终点为1年后的无进展生存期(PFS)。次要终点为缓解率、无事件生存期(EFS)(至进展、复发、死亡或非计划抗淋巴瘤治疗的时间)、总生存期(OS)和毒性。研究方案规定,在前180例患者完成至少1次随访调查后,进行预先计划的期中分析。
研究结果
2018年1月-2021年5月,共180例患者纳入本研究,患者的基线特征如表1所示。2例患者未接受任何治疗(1例撤回知情同意,1例死亡),因此全分析集为n=90(A组)和n=88(B组)。中位年龄76岁(范围44-87岁),52%的患者年龄>75岁,37%的患者为一线治疗后原发性进展,62%的患者IPI评分为3-5。
表1
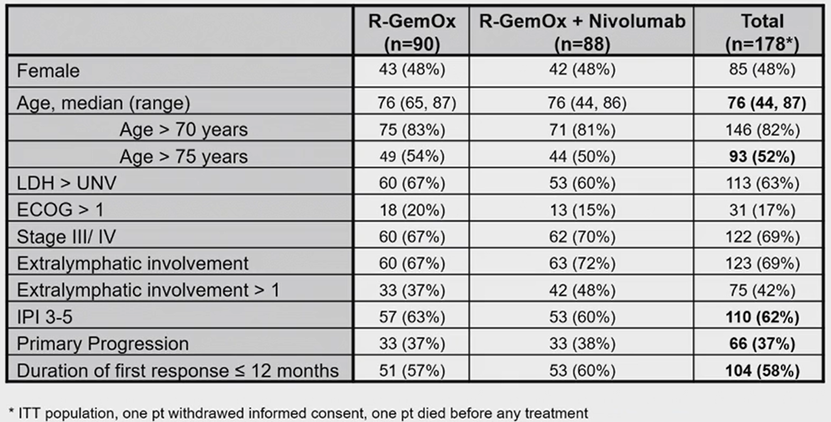
两组的ORR和CR率相似,分别为34%和20%(A组)vs. 34%和22%(B组)。疾病进展(PD)率为53%(A组)和50%(B组)。中位随访21个月之后,1年PFS率为28%(95%CI:18%-37%)(A组)vs 20%(95%CI:11%-28%)(p=0.827)(B组)。1年EFS率为22%(95%CI:13%-31%)(A组)vs 20%(95%CI:11%-28%)(p=0.654)(B组)。一年OS率为48%(95%CI:38%-59%)(A组)vs 58%(95%CI:47%-68%)(p=0.126)(B组)。2年的PFS率、EFS率和OS率分别为15%(95%CI:6%-24%)、13%(95%CI:5%-21%)和34%(95%CI:22%-46%)(A组)vs 15%(95%CI:7%-23%)、15%(95%CI:7%-23%)和43%(95%CI:32%-55%)(B组)。
由于PFS相同但B组的OS有更好的趋势,因此研究者对第二次疾病进展/复发的患者(A组70例,B组73例)进行了OS分析。第二次进展/复发后,B组的OS率优于A组(对数秩p=0.010)(图1)。
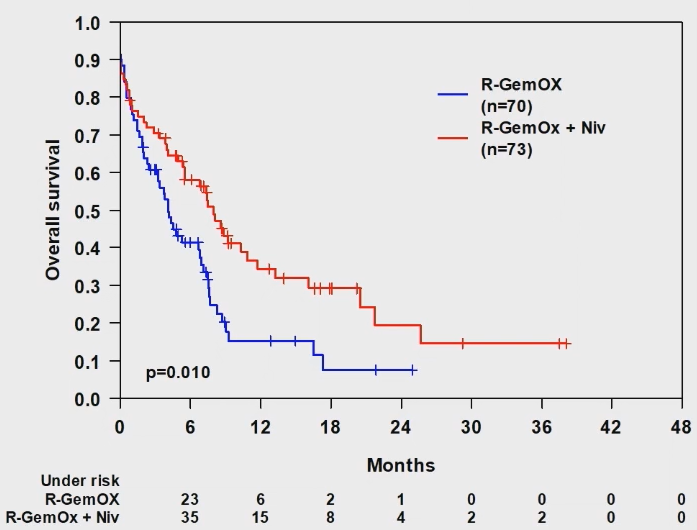
图1
B组出现3-5级不良事件(AE)的患者人数略有增加(A/B组:血小板减少37%/39%;贫血19%/26%;白细胞减少19%/24%;感染15%/22%)。除脂肪酶(A/B组:23%/27%)(p=0.625)和淀粉酶(A/B组:5%/11%)(p=0.192)无症状性升高外,免疫相关3-5级AE的数量没有增加。B组患者在纳武利尤单抗巩固治疗期间最常见的3-5级AE为白细胞减少(13%)、周围神经病变(10%)、脂肪酶升高(8%)、贫血(5%)和感染(5%)。共发生了7例治疗相关死亡(A/B组:3例[3%]/4例[5%])(图2)。
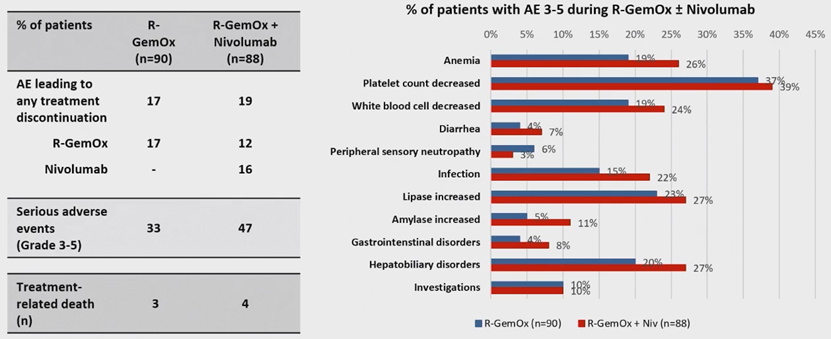
图2
102例患者在复发/进展后接受了挽救治疗,治疗方案如表2所示。研究者对复发/进展以及接受挽救治疗的患者亚组进行了分析(图3)。
表2
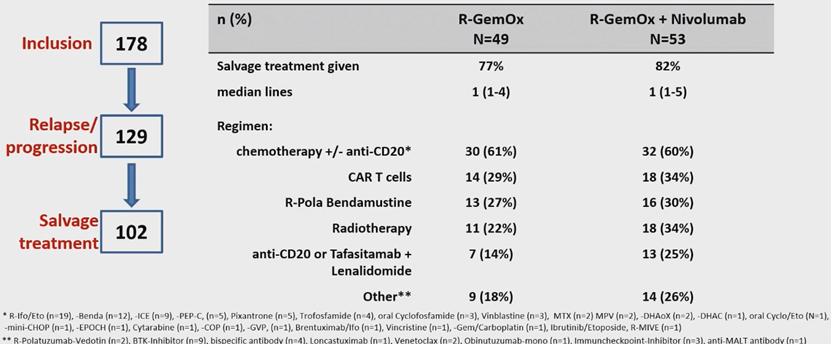
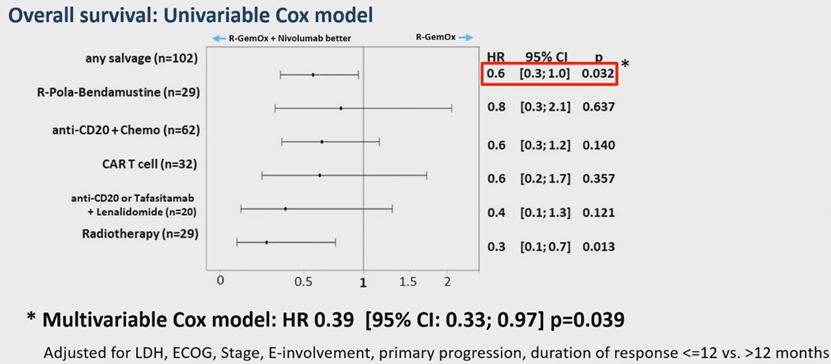
图3
此项期中分析无法证明在主要终点方面的优效性,因此于2023年3月停止了患者招募。最初计划的310例患者中有270例被招募。
研究结论
对于R/R LBCL患者,在R-GemOx基础上加用纳武利尤单抗,随后纳武利尤单抗维持治疗是可行的,且无相关附加毒性。加用纳武利尤单抗未能改善R-GemOx单独治疗方案的PFS。这些结果表明,接受免疫化疗的R/R不适合移植的患者预后不良。在第二次复发/进展和接受其他治疗的患者亚组中,纳武利尤单抗显著提高了后续治疗的疗效,结果将在最终分析(n=270)中得到证实。
02 Epcoritamab SC联合GemOx治疗不适合ASCT的R/R DLBCL患者可获得高完全代谢缓解率:EPCORE NHL-2研究的最新结果
Epcoritamab是皮下注射(SC)的CD3xCD20双特异性抗体,在EPCORE NHL‑2 I/II期试验(NCT04663347)中,在失败或不适合接受ASCT的R/R DLBCL患者中,Epcoritamab联合GemOx治疗显示出令人鼓舞的初步疗效,总体安全性符合预期且可控。本次ASH大会研究者报告了随访时间较长的最新结果。该研究纳入了ASCT失败或不适合ASCT的R/R CD20+ DLBCL成人患者。患者接受Epcoritamab SC:每28天为1个周期;每周一次,C1-3;每2周一次,C4-9;每4周一次,C≥10,直至疾病进展或出现不可接受的毒性。C1-4,患者每2周接受1次GemOx治疗。在C1中,患者需要接受Epcoritamab阶梯剂量给药(递增剂量1和2,随后48mg全剂量)和皮质类固醇预防,以减轻细胞因子释放综合征(CRS)。主要终点是根据Lugano标准通过PET-CT评估的ORR。
研究结果
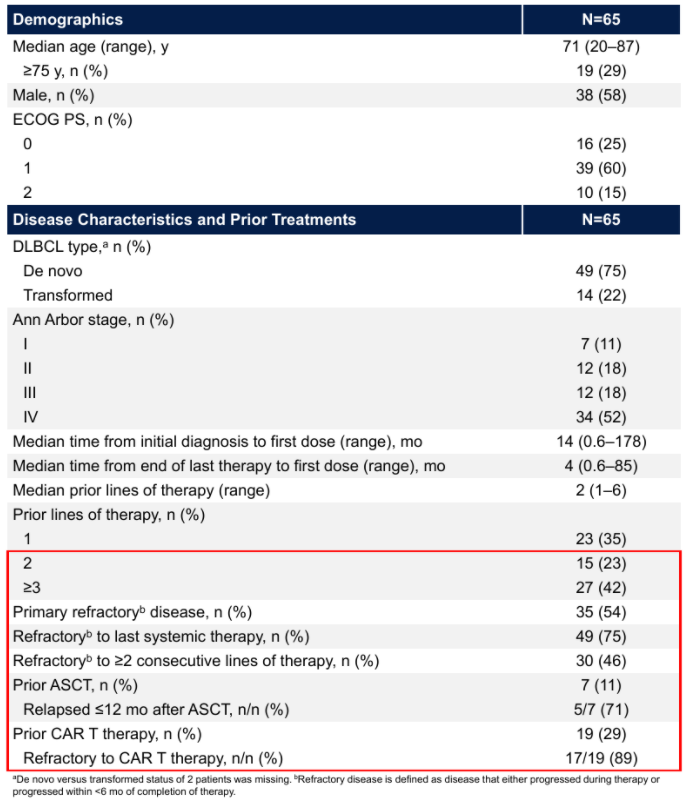
研究共纳入65例患者,患者的基线特征如表3所示。中位年龄71岁(范围,20-87),中位随访11.4个月(范围,1.0+-30.6)。数据截止日期为2023年9月1日,大多数患者(70%)为III或IV期疾病,54%为原发性难治性疾病,46%对既往连续≥2线治疗难治,75%对最后一线治疗难治。既往中位治疗线数为2(1-6),27例患者(42%)既往接受过≥3线治疗。共计19例(29%)患者既往接受过CAR-T治疗,7例(11%)患者既往接受过ASCT。
表3
治疗中最常见的(>20%)任何级别的治疗期间出现的不良事件(TEAE)如图4所示。4例患者出现发热性中性粒细胞减少,2例患者报告ICANS(1级和3级),两起事件均得到缓解,1例患者因ICANS停止治疗。未报告临床肿瘤溶解综合征。本试验在全球COVID-19大流行期间开展,受到流行的COVID-19趋势的影响,包括高传染性的奥密克戎变异株。11例患者发生5级TEAE,4起事件与COVID-19相关,2例患者研究者无法排除Epcoritamab的作用。
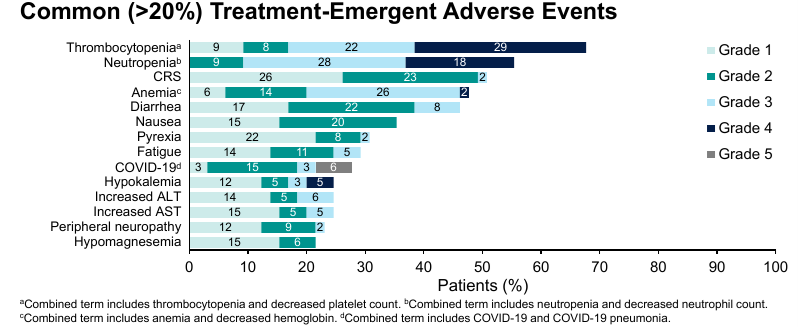
图4
大多数CRS事件为低级别(49%为1-2级,2%为3级),主要发生在第1次全剂量(C1D15)后,未发生导致Epcoritamab停药的CRS,所有事件均缓解(图5)。
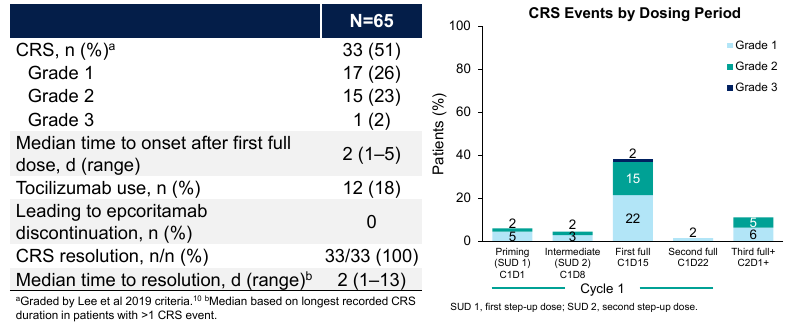
图5
ORR为80%(52/65),57%(37/65)的患者达到完全代谢缓解(CMR)(表4)。中位至缓解和CMR的时间分别为1.5个月和1.8个月。
表4

在原发性难治性疾病患者中,ORR和CMR率分别为74%和40%,在≥75岁患者中,ORR和CMR率分别为89%和79%,在IPI>3的患者中,ORR和CMR率分别为75%和50%。既往接受过CAR-T治疗的患者的ORR为63%,CMR率为42%;未接受过CAR-T治疗的患者的ORR为87%,CMR率为63%(图6)。
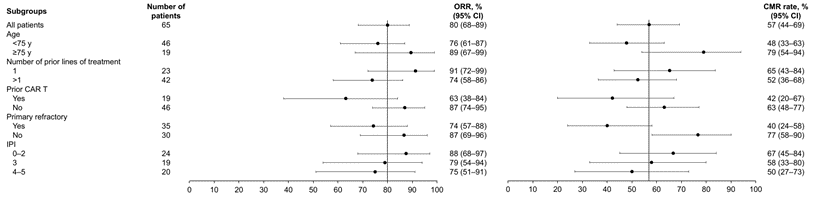
图6
研究结论
Epcoritamab SC联合GemOx在不适合移植且医疗需求高的R/R DLBCL患者中获得了较高的ORR和CMR率,缓解程度深且持久,中位CMR持续时间为13.3个月,中位OS未达到。在各亚组中均观察到较高的ORR和CMR率,并且在二线和未接受CAR-T治疗的患者中显著较高。本试验未发现新的安全信号,且安全性与各药物的安全性一致。这些数据令人鼓舞,突显出Epcoritamab SC用于治疗R/R DLBCL的多功能性。